מחקר בגובה העיניים
מחקר בגובה העיניים
עובדות ומספרים

מנסים להיאבק במחלות ניווניות של המוח
חוקרים פגעו במסלול גנטי מקדם הזדקנות בגופן של תולעים, וכך מנעו מחלבון שקשור באלצהיימר להרוס את תאי העצב שלהן
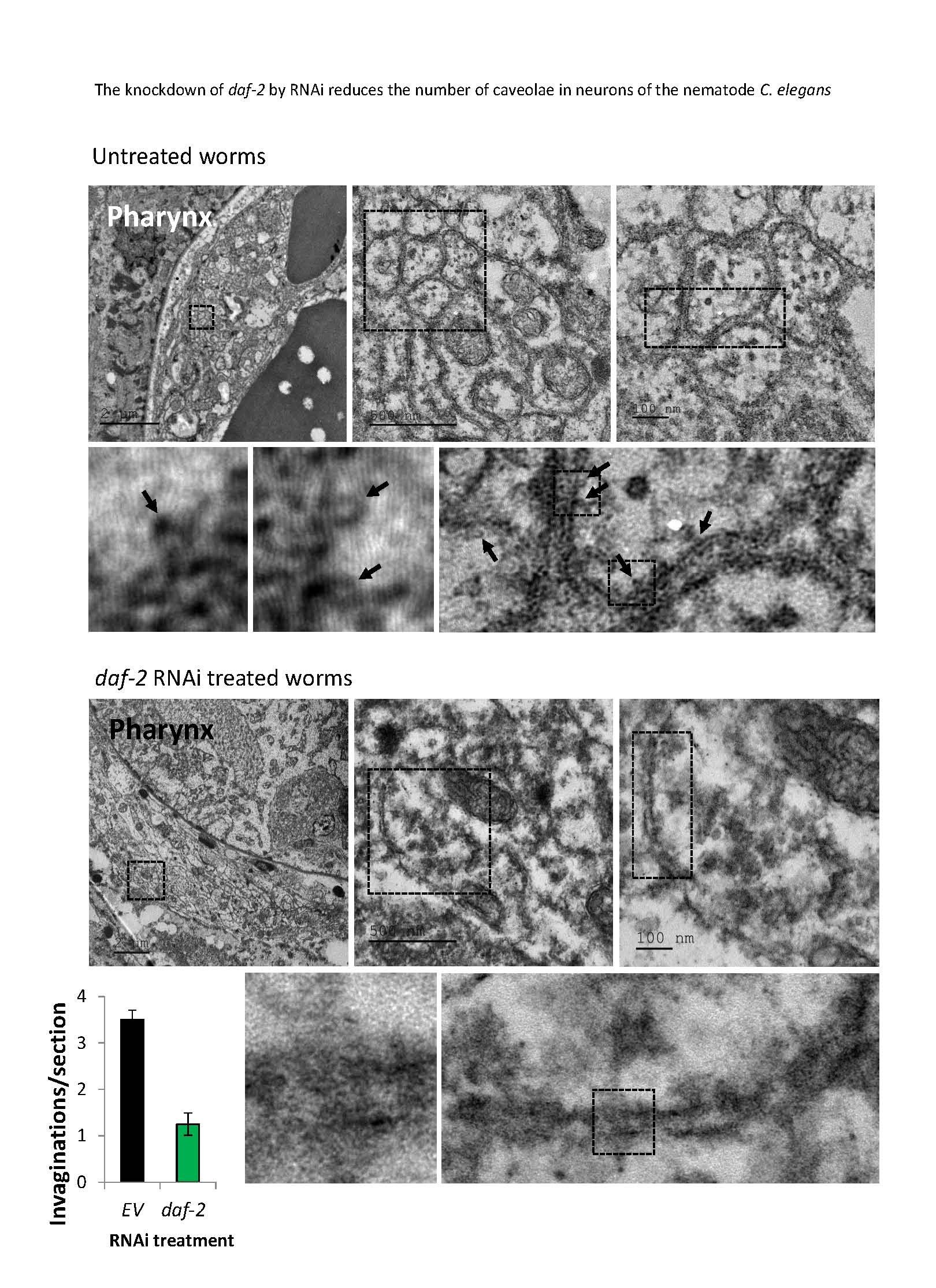
מחלות ניווניות של המוח שמתפתחות עם הגיל מתאפיינות בהתנוונות תאי עצב ובמותם. כמעט כל המחלות הללו חשוכות מרפא, והטיפול בהן יכול בעיקר להאט את התקדמותן או להפחית את התסמינים שנגרמים מהן. הידועות שבמחלות אלו הן אלצהיימר ופרקינסון. אלצהיימר מתאפיינת בירידה בתפקוד קליפת המוח ובהידרדרות קוגניטיבית ומנטלית; ופרקינסון היא אחת מהפרעות התנועה הנפוצות ביותר. הפתולוגיה העיקרית והידועה שלה היא התנוונות של תאי עצב שנמצאים בגזע המוח. אחת הסיבות המרכזיות הידועות שמובילות למחלות כגון אלו היא הצטברות של חלבונים שהמבנה התקין שלהם נהרס (אינם מקופלים נכון); הם שוקעים בין תאי העצב במוח והללו אינם מסוגלים לפרקם ובסופו של דבר נהרסים. הופעת המחלות הללו בגיל מבוגר עשויה להעיד על כך שתאי הגוף המזדקנים לא מצליחים לדכא את הצטברות החלבונים הפגומים בין תאי העצב. זאת מכיוון שעם הגיל פוחתת יכולתם לשמר את תקינות החלבונים. כך למשל, נפגעת פעילותם של חלבונים שמסייעים לחלבונים אחרים להתקפל נכון ופעילותם של חלבונים שמזהים חלבונים פגומים וגורמים לפירוקם. במעבדתנו אנו מנסים להפחית את פעילות המסלולים הגנטיים שמזקינים את האורגניזם. זאת מתוך תפיסה שכך נצליח למנוע את הצטברות החלבונים הפגומים במוח. במחקרים קודמים שעשינו על תולעים עגולות (נמטודות), גילינו כי הפחתת פעילות של מסלול העברת אותות על ידי ההורמון אינסולין והורמון הגדילה IGF1 – הידוע כמקדם הזדקנות (ככל שהורמונים אלו נקלטים יותר בתאים – הם מזדקנים יותר, ובהתאמה מתפתחות מחלות הקשורות בגיל כגון סרטן וסוכרת) – הצליחה להגן מפני הצטברות של עמילואיד-בטא בתאי עצב במוח. חלבון זה נמצא קשור לירידה הקוגניטיבית שחלה באלצהיימר. כאשר הוא שוקע בין תאי העצב במוח הוא גורם להפרעה בתקשורת ביניהם. נמטודות הן חיית מודל מצוינת לתחום זה שכן יש להן כ-300 תאי עצב, בהם חישתיים, וקיים מידע רב על הקשרים (מעבר של אותות כימיים וחשמליים) ביניהם. בנוסף, תוחלת חייהן קצרה וניתן לבצע בהן מניפולציות של הזדקנות בקלות יחסית. במחקר זה המשכנו לחקור כיצד ניתן להגן עליהן מפני הצטברות של חלבונים רעילים ברקמות שונות. חקרנו נמטודות שהונדסו לבטא את החלבון עמילואיד-בטא. חילקנו אותן לשתי קבוצות: קבוצת ביקורת שלא עברה כל התערבות וקבוצת ניסוי שעברה טיפול באמצעות שיטות גנטיות (הפחתת ביטוי של גנים וחלבונים); בטיפול זה פגענו במסלול העברת האותות על ידי ההורמון אינסולין והורמון הגדילה IGF1, וגילינו בשיטות מולקולריות שכך פחתה רמת ביטויו של חלבון ששמו קוואולין (הגן שמייצר קוואולין מבוקר על ידי חלבונים שמבוקרים על ידי הקולטן ל-IGF1). דבר זה הפחית את מספר המבנים שאותו חלבון חיוני לייצורם – קוואולות שמם – שקיימים בתאי עצב. הקוואולות הן פלטפורמה להתארגנות של קומפלקסים חלבוניים וייתכן כי הן משמשות גם מקום לשקיעת החלבונים הפגומים. במעקב שביצענו לאורך חייהן של הנמטודות, ראינו כי בקבוצת הניסוי – הפגיעה בייצור הקוואולות תרמה להגנה מפני רעילותו של העמילואיד-בטא; חשפנו את הנמטודות לחומרים שלרוב גורמים להן לרתיעה, וראינו שהן אכן התרחקו מהם. כלומר: תאי העצב שלהן, שחלקם כאמור חישתיים, תפקדו באופן תקין. זאת לעומת תולעי קבוצת הביקורת – הן לא נמנעו מאותם חומרים, מה שכפי הנראה מעיד על הצטברות העמילואיד-בטא שפגעה בתפקוד תאי העצב. כך למעשה, באמצעות הפגיעה במסלול האותות, מנענו מהחלבון הפגום לפגוע בתאי העצב, ואנו מקווים שבעתיד פעולה זו תוכל להיות טיפול יעיל לחולים במחלות ניווניות של המוח.
תמונות המחקר













 מועדי הגשת בקשות
מועדי הגשת בקשות
 ערוצי תמיכה
ערוצי תמיכה
 הודעות הקרן
הודעות הקרן
 תהליך הגשת בקשות
תהליך הגשת בקשות
 תהליך השיפוט
תהליך השיפוט
 נתונים על פעילות הקרן
נתונים על פעילות הקרן
 שיחות עם חוקרים
שיחות עם חוקרים
 צרו קשר
צרו קשר




